最新の研究
- 2018.02.01
- 山口・黒木研究室
疾患診断に向けた生体分子認識ゲート膜の汎用化・高感度化
後期高齢社会の到来に伴い、病気の早期発見や健康増進のために、在宅やベッドサイドなどで、簡単かつ迅速に行う医療検査(Point-of care testing, POCT)が重要となります。このPOTCの実用化のためには、バイオマーカーと呼ばれる、特定の病気の時にのみ体内へ放出される生体分子を、簡便かつ迅速に標的分子シグナルを検出するデバイス開発が必要です。
このような性能を有するデバイスの一つとして、多孔質膜中の細孔を標的分子の認識場として利用した膜型センサーが研究されています。我々は、生体分子の多点認識・架橋により、細孔の開放・閉塞を制御する新しい膜型センサーを開発してきました[1]。この生体分子認識ゲート膜は、標的分子に対するセンサー部位と感温性高分子の共重合グラフトポリマーを多孔質膜の細孔中に固定したものです。この膜では、標的分子存在時のみ、特異的に多点で捕捉された標的分子によって、細孔中のグラフトポリマー間で架橋が形成されます。この状態で温度シグナルを与えて、グラフトポリマーを収縮させても、標的分子認識時のみ細孔の閉塞が維持され、この変化を、水透過性の変化で検出することが可能です。化学工学計算から、膜構造を最適化することで、既往の診断法以上の感度(pMレベル)にまで高められることが明らかになっており、POCT用デバイスへの応用が期待されます。我々は、この生体分子認識ゲート膜の汎用化・高感度化に向けて、細孔内へのセンサー部位導入法と標的分子認識法の検討を行いました[2]。
細孔内のグラフトポリマー中に、マイルドな環境で進行する高効率な反応でセンサー部位を導入することができれば、導入できるセンサー部位の幅を格段に拡げることができ、汎用性が高くなります。そこで、高反応性・高選択性なClick反応の一つであるフィスゲン環化付加反応[3, 4]を用いて、細孔へのセンサー部位の導入を行いました。具体的には、多孔質ポリエチレン基材の細孔中に、プラズマグラフト重合[5, 6]を用いて、感温性部位となるN-isopropyl acrylamide (NIPAM)とセンサー導入部位となるglycidyl methacrylate (GMA)の共重合ポリマーを固定した後、GMAのエポキシ基に末端アルキン基を導入し、Click反応を用いてセンサー部位であるビオチンを導入しました(図1)。FT-IRと重量変化により、ビオチン部位が90%と高効率に導入できていることを確認しました。
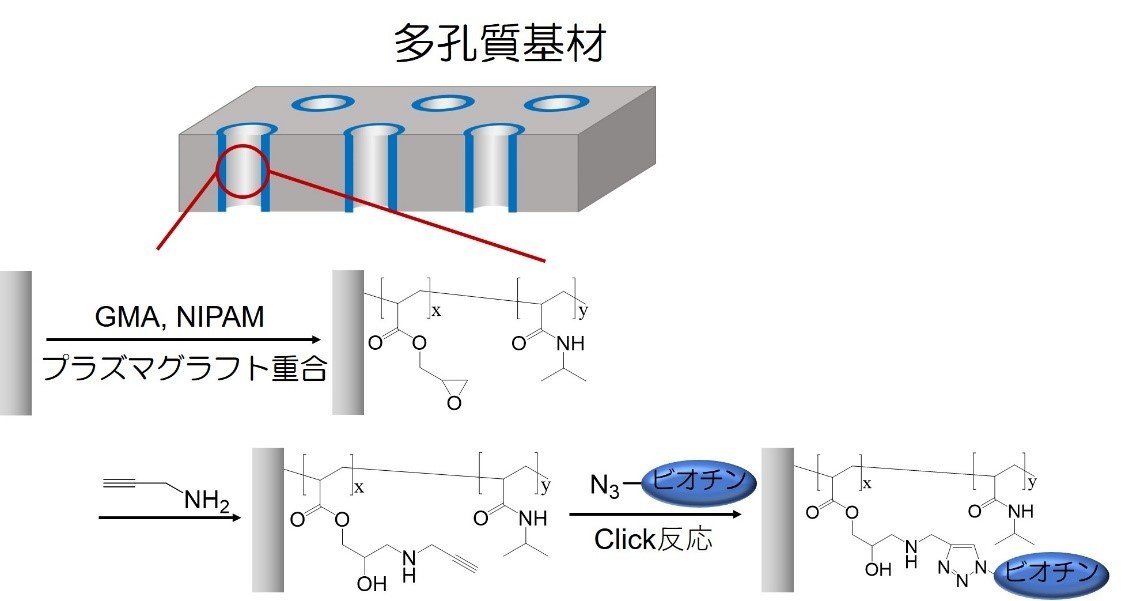 図1 Click反応を用いた多孔質基材細孔内へのセンサー部位導入法
図1 Click反応を用いた多孔質基材細孔内へのセンサー部位導入法
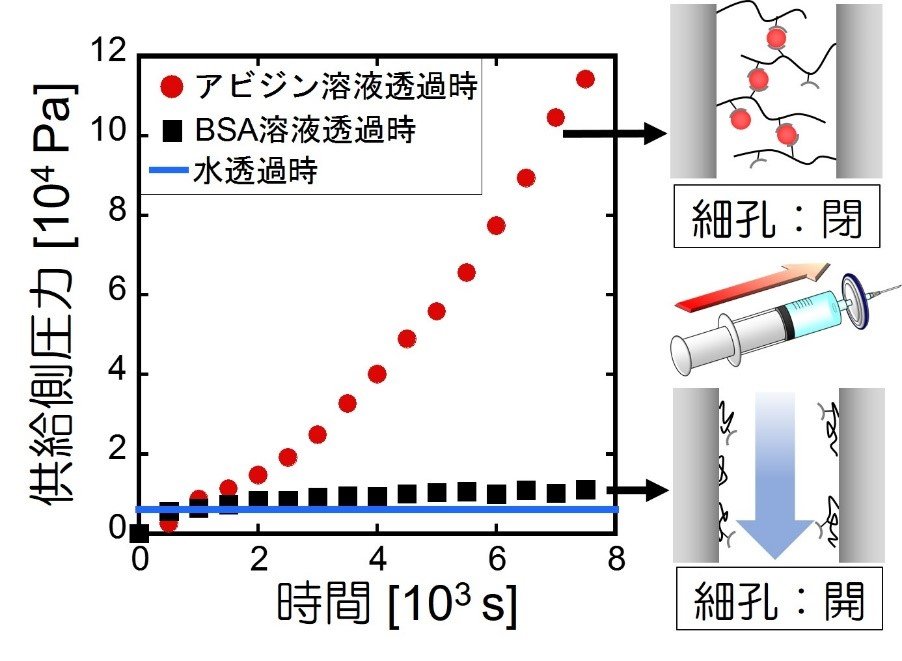
これまでの生体分子認識ゲート膜では、膜を検体溶液へ浸漬することで標的分子の認識を行っています(含浸法)が、対流を使って標的分子を細孔へ導入することができれば、標的分子とレセプター分子の接触頻度が向上し、感度が大幅に改善されることが期待されます[7]。そこで、作製したゲート膜に検体溶液を透過させることで、細孔内に標的分子を積極的に送り込む効率的な分子認識法(透過法)の検討を行いました。標的分子であるアビジン、コントロールとしてウシ血清アルブミン(BSA)を用いて、一定流束に対する供給圧の変化を装置内の圧力センサーによって測定しました。図2に、45oCにおける水透過時、BSA透過時、アビジン透過時の圧力変化を示します。BSA水溶液透過時の圧力は水透過時と同様に低い値であり、細孔中で分子認識が行われず、水透過時と同様に開いた状態です。一方で、アビジン水溶液透過時には、圧力が時間と共に大きく上昇していることから、細孔中における分子認識とそれに基づくポリマー間多点結合によって膜細孔が次第に閉塞していくことが示されました。
次に、供給側圧力で規格化した透過流束の逆数を透過抵抗Rと定義し、透過法とこれまでの含浸法とで比較を行いました(図3)。含浸法でのBSA透過後とアビジン透過後における透過抵抗比は約2倍であるのに対し、透過法では透過性比が約30倍と高い差が示されました。両手法で用いた検体溶液中のアビジン濃度は等しく、また透過法でのアビジン溶液の接触時間は含浸法に比べて4倍短いことを考慮すると、透過法を用いることによって高感度なセンシングが達成可能であることを示しています。これは、細孔内にアビジン分子を積極的に透過させることにより、溶液中・膜細孔内の拡散律速が解消され、細孔内のビオチンにアクセスしやすくなったためと考えられます。
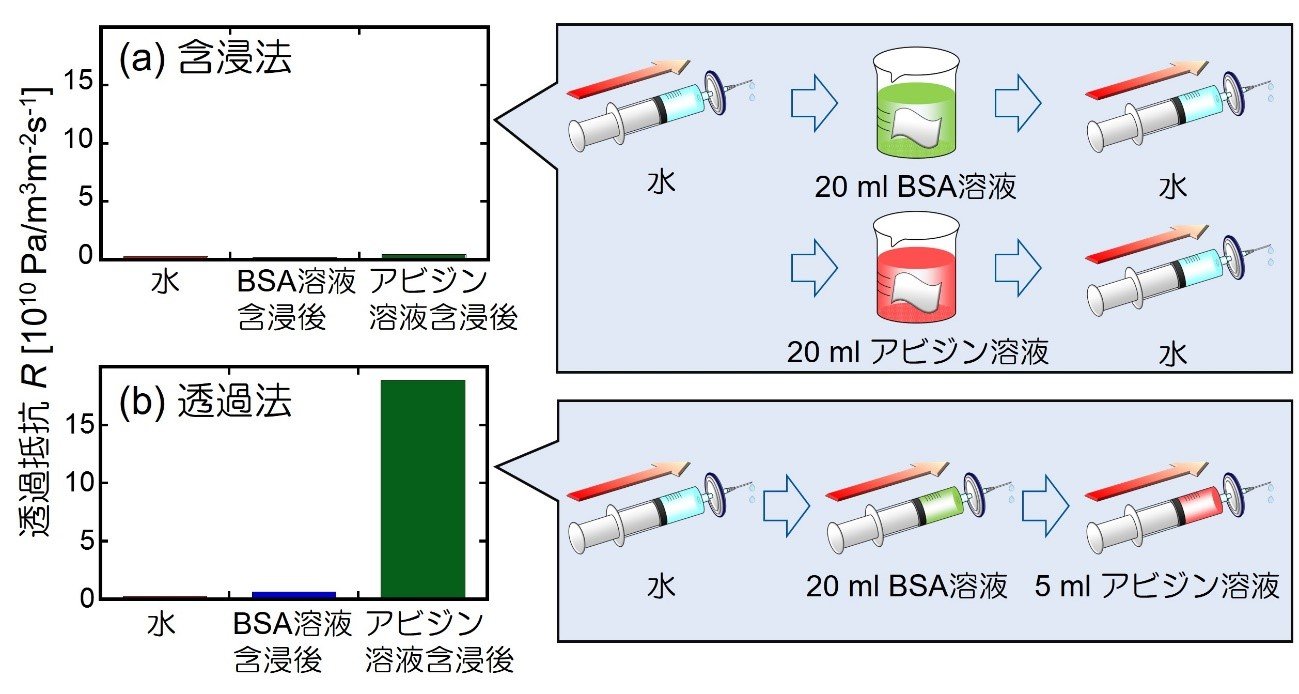 図3 45 oCにおける各溶液認識前後での透過抵抗(a)含浸法、(b) 透過法
図3 45 oCにおける各溶液認識前後での透過抵抗(a)含浸法、(b) 透過法
本稿で紹介したClick反応を用いたゲート膜作製法により、今後はビオチンに限らず、マイルドな条件での導入が必要な、ポリクローナル抗体やDNAなど種々のセンサー分子が高効率に導入できると期待されます。また、標的分子溶液を対流により細孔内に積極的に浸透させる透過法は、温度シグナルをかけることなく、より簡便で効率的・高感度な分子認識を可能にすることから、生体分子認識ゲート膜の可能性を大きく拡げ、POCTに向けた有効な手法になると考えています。
引用文献
1) H. Kuroki, T. Ito, H. Ohashi, T. Tamaki, T. Yamaguchi, Anal. Chem., 83, 9226(2011).
2) H. Okuyama, Y. Oshiba, H. Ohashi, T. Yamaguchi, Small, in press.
3) H. C. Kolb, M. G. Finn, K. B. Sharpless, Angew. Chem.-Int. Edit., 40, 2004(2001).
4) J. F. Lutz, Angew. Chem.-Int. Edit., 46, 1018(2007).
5) T. Yamaguchi, S. Nakao, S. Kimura, Macromolecules, 24, 5522(1991).
6) X. Q. Chi, H. Ohashi, T. Yamaguchi, Plasma Process. Polym., 11, 306(2014).
7) J. H. Dai, G. L. Baker, M. L. Bruening, Anal. Chem., 78, 135 (2006).