最新の研究
- 2020.10.01
- 北口研究室
抗体の極めて簡便な蛍光センサー化に成功
-各種低分子の高感度かつ簡便な検出が可能に-
抗体を用いた免疫測定法は,サンプル中の微量物質の特異的かつ高感度な検出法として,臨床診断から環境分析や食品衛生など様々な分野で利用されている。特に最近では感染症における抗原・抗体の迅速診断技術として免疫測定法の一種であるイムノクロマト法が注目されている。しかし,より高感度なELISA法を含め,感度と測定の簡便さの両立が難しい問題を抱えており,簡便迅速高感度な免疫センサーの実現が待たれていた。
我々は数年前,抗体のアミノ末端近傍を蛍光標識することで,サンプルと混ぜて数分後に蛍光を測定するだけで抗原を高感度に定量可能な免疫センサータンパク質,クエンチ抗体(QuenchbodyあるいはQ-body)の構築に成功していた(図1)[文献1]。Q-bodyにおいては,抗原不在時には色素は抗体内部に取り込まれて抗体内のトリプトファン残基からの光誘起電子移動PeTにより蛍光色素がクエンチ(消光)されるが,抗原添加により色素が抗体外に移動することで蛍光を発する[文献2]。リンカー長を変化させたり色素を複数導入するなどの工夫の結果,低分子からタンパク質まで,これまで多くの抗原の高感度検出に成功してきた。しかし,多くの場合,これらは手間のかかる抗体遺伝子クローニング,大腸菌での組換えタンパク質発現と色素の化学修飾を介して構築しなければならず,更に構築してみないとその性能が予測できない問題があった。
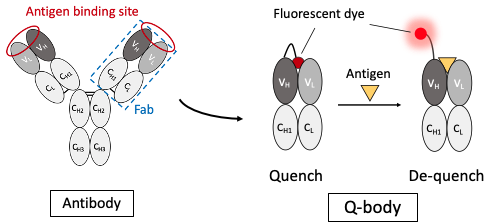
図1. 蛍光色素で標識した抗体断片バイオセンサー,クエンチ抗体。TAMRAなど抗体に付加した色素は,Trp残基によって蛍光が消光され,抗原が結合すると蛍光が回復する。この方法により,迅速簡便に標的を検出できる。
我々は今回,抗体結合タンパク質プロテインM (PM)を用いて,市販抗体など多くの抗体を簡便に蛍光バイオセンサー化可能なプローブ(PM Q-probe)の開発に成功した[文献3]。PMは,最近マイコプラズマから発見された抗体L鎖結合タンパク質である[文献4]。幅広い種の抗体と強く結合し,構造的に抗原との結合をブロックし免疫系を撹乱するとされている。我々は,このPMのC末端が抗体結合時にその抗原結合部位に近づくこと,また抗原が低分子であればその結合が邪魔されないのではとの推測から,PMのC末端側に短いリンカーを介して色素を導入したプローブを構築し,PM Q-probeと命名した(図2)。このQ-probeは,モデルとして用いた骨疾患マーカーであるオステオカルシン認識抗体Fab断片あるいは全長IgG抗体と混合すると蛍光が約50%クエンチされ,これらにさらに抗原を添加すると蛍光が元に回復するなど,Q-bodyとほぼ同等の性質を持つ事を見いだした。さらに興味深い事に,IgGとの複合体は組換え法により構築したFabより高い抗原検出感度を示した(図3)。
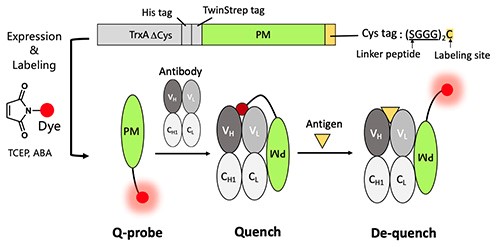
図2. C 末端に蛍光色素で標識した抗体結合タンパク質であるクエンチプローブ(Q-probe)。構築のスキームと予想されるクエンチ・脱クエンチ機構を示す。
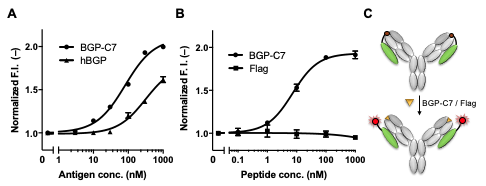
図3. 組換えFab(A)と天然型IgG(B,C)によるBGP-C7抗原の検出。Flagペプチドは陰性対照。AではhBGPの反応性が低いが,これは組換えQ-bodyでも見られる現象である。
そこで,次に市販の抗体を含む各種IgGを用いて,血中診断に用いられる黄体ホルモン,男性ホルモン,甲状腺ホルモンT4など多くの低分子バイオマーカーの濃度測定を試みた所,それぞれ健常人の血中濃度が検出可能な感度で定量できた。また,血清からエタノールを用いて抽出したT4濃度を定量することにも成功した。すなわちこの方法で,血中タンパク質に結合したT4を含む総T4濃度の測定に成功した(図4)。しかし,血清サンプルの直接測定は,血清中の抗体の影響によりQ-probe/IgG複合体が解離するため困難であった。
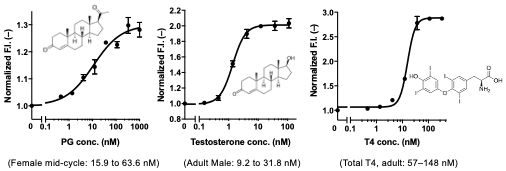
図4. Q-probe/IgG複合体によるステロイドホルモン(プロゲステロン,テストステロン,チロキシン)の検出。血清中の正常濃度範囲も示す。
そこで血清中のホルモン量を直接測定するため,ストレスホルモンとして知られるコルチゾールに対する抗体4種を材料として,Q-probeで高い応答を示した1種の抗体について,抗体産生細胞から遺伝子工学的にコルチゾールに対するQ-bodyを構築した。こうして構築したQ-bodyは,Q-probe/IgG複合体と同様の蛍光応答を示し,さらに50%血清中での測定において緩衝液中と同等以上の性能を示した(図5)。すなわち,Q-probeがQ-body化に適した抗体の選別に使える事と,その結果得られたQ-bodyが血清中抗原の直接測定に使える事が判明した。
以上の結果は,本技術によりQ-bodyの応用範囲が広がり,各種分子の蛍光検出が従来よりはるかに簡便化できる可能性を示している。
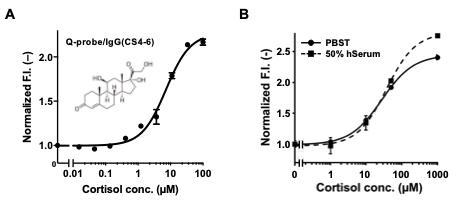
図5. 抗CS IgGのQ-bodyへの変換。Q-probe/IgG複合体(A)とscFv型Q-body(B)によるコルチゾールの検出。 Bは,50%ヒト血清中での検出も示す。
参考文献
| [1] | R. Abe, H. Ohashi, I. Iijima, M. Ihara, H. Takagi, T. Hohsaka, H. Ueda. J. Am. Chem. Soc. 2011, 133, 17386-17394. |
| [2] | H. Ohashi, T. Matsumoto, H.-J. Jeong, J. Dong, R. Abe, and H. Ueda, Bioconj. Chem., 2016, 27, 2248-2253. |
| [3] | J. Dong, C. Miyake, T. Yasuda, H. Oyama, I. Morita, T. Tsukahara, M. Takahashi, H.-J. Jeong, T. Kitaguchi, N. Kobayashi and H. Ueda Biosens. Bioelectron. 2020, 165, 112425, Pat. P. WO/2018/147018 (Tokyo Tech). |
| [4] | Grover, R. K., et al.: Science, 2014, 343, 656-661. |



