最新の研究
- 2022.01.13
- 福島・庄子研究室
ホウ素-ホウ素結合の回転が織りなす二重蛍光と溶媒粘度センシング機能
ホウ素化合物の構造や性質は、その電子欠損性とホウ素の低い電気陰性度に特徴づけられます。例えば中性3配位のホウ素化合物はボランと呼ばれ、ホウ素原子上に空の2p軌道があるため強いルイス酸性・電子受容性を示します(図1a)。我々は、ホウ素の空軌道の特性を最大限に活用できる化学種の創製と反応開発に取り組んできました。これまでに開発した化合物の例に、ホウ素が結合の手を2本しかもたないカチオン性化合物「ボリニウムイオン」があります(図1a,b)[1]。このボリニウムイオン(Mes2B+)は、CO2の安定なC=O二重結合を室温で容易に切断するなど、特異な反応を示すことがわかっています。Mes2B+ の興味深い性質は、ホウ素原子上に二つの空の2p軌道をもつ異常な電子欠損構造にあると考えられます。
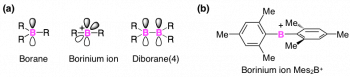 |
|
| Fig. 1. |
(a) Schematic illustrations of boron species. The lobes on the boron atoms represent vacant 2p orbitals. (b) Chemical structure of diarylborinium ion Mes2B+.
|
二つ空の2p軌道が相関したホウ素化合物の他の例として、ホウ素-ホウ素結合を有するジボラン(4)が挙げられます(図1a)。ビス(ピナコラート)ジボロンに代表されるように、これまでに報告されているジボラン(4) 誘導体のほとんどは、ホウ素原子上の置換基から電子対を受け取り安定化されたものでした。一方、ホウ素上に芳香環のみが置換したテトラアリールジボラン(4) 誘導体も数例報告されていますが、いずれも、大気中で容易に加水分解され分解してしまいます[2]。ジボラン(4)がもつ隣り合った二つの空軌道の性質を引き出すためには、電子対を供与できる置換基を使わず、かつ化学的安定性を実現できる分子設計が望まれます。
その糸口となったのが、前述のボリニウムイオン Mes2B+ です。我々は、このMes2B+ をリチウム金属で還元すると、分子間でホウ素-ホウ素結合が形成されることを見いだしました。この新規合成法により、4つのメシチル基(2,4,6-トリメチルフェニル基)で高度に立体保護されたテトラアリールジボラン(4) Mes4B2 を合成することに成功しました(図2a)[3]。 Mes4B2 の結晶構造を見ると、ホウ素-ホウ素結合がメシチル基でほぼ完全に覆われています(図2b)。特筆すべきことに、Mes4B2 は、テトラアリールジボラン(4)としては例外的に水中でも分解しません。この優れた化学安定性により、Mes4B2 の性質を詳細に調べることが可能になりました。
 |
|
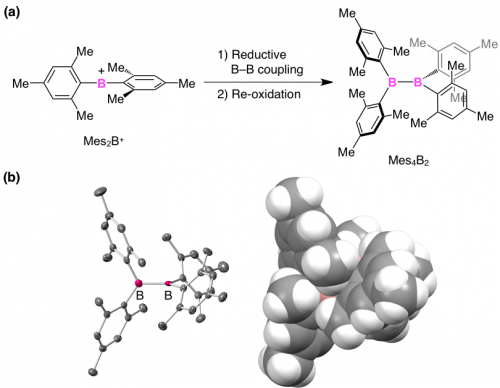
| Fig. 2. |
(a) Synthesis of tetraaryldiborane(4) Mes4B2 by the reductive coupling of borinium ion Mes2B+. (b) Crystal structure of Mes4B2 (left: thermal ellipsoid, right: CPK description).
|
興味深いことに、Mes4B2は鮮やかなオレンジ色の蛍光発光を示しました。Mes4B2のシンプルな分子構造からは予想していなかった挙動です。Mes4B2の発光挙動をより詳しく調べると、観測されたオレンジ色の蛍光発光には、強度の小さい短波長側(λmax = 460 nm)と、強度の大きい長波長側(λmax = 620 nm)の二つの発光帯が含まれていることがわかりました(図3a)。すなわち、Mes4B2は二重蛍光を示します。
 |
|
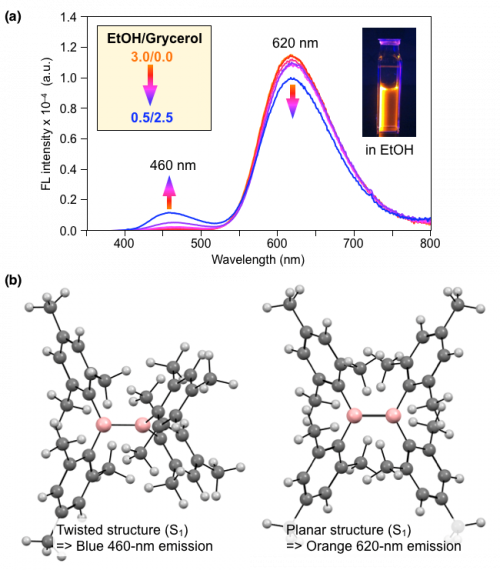
| Fig. 3. |
(a) Fluorescence spectra of Mes4B2 in in ethanol/glycerol (3.0/0.0 to 0.5/2.5 v/v) at 25 °C (Λex = 360 nm).
(b). Calculated equilibrium structures of Mes4B2 in the excited S1 state. |
Mes4B2の発光挙動を理解するために、基底(S0)
この計算結果から予想されるように、Mes4B2の二重蛍光の相
Mes4B2の二重蛍光挙動は、
Fig. 4. Photographs of an evaporated film of Mes4B2 before and after annealing at 80 °C
以上、高い化学的安定性をもったMes4B2の合成に成功し、
ジボラン(4)の研究以外にも、
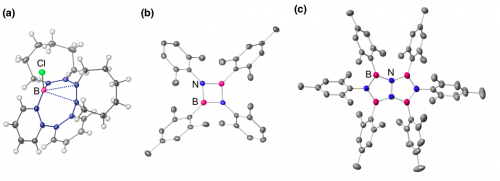
Fig. 5. (a) Boron-containing macrocycle exhibiting a strong borane-olefin proximity interaction[4]. (b) B2N2-heterocyclobutadiene emitting blue phosphorescence in solution at room temperature[5]. (c) B4N4-heteropentalene that can serve as a host material for OLED[6].
References
| [1] | Y. Shoji, N. Tanaka, K. Mikami, M. Uchiyama, T. Fukushima, Nat. Chem. 2014, 6, 498-503. (https://www.nature.com/ |
| [2] | (a) A. Moezzi, M. M. Olmstead, P. P. Power, J. Am. Chem. Soc. 1992, 114, 2715-2717. (b) N. Tsukahara, H. Asakawa, K.-H. Lee, Z. Lin, M. Yamashita, J. Am. Chem. Soc. 2017, 139, 2593-2596. (c) T. Araki, M. Hirai, A. Wakamiya, W. E. Piers, S. Yamaguchi, Chem. Lett. 2017, 46, 1714. (d) F. Ge, X. Tao, C. G. Daniliuc, G. Kehr, G. Erker, Angew. Chem. Int. Ed. 2018, 57, 14570-14574. |
| [3] | Y. Shoji, N. Tanaka, Y. Ikabata, H. Sakai, T. Hasobe, N. Koch, H. Nakai, T. Fukushima, Angew. Chem. Int. Ed. 2022, 61, e202113549. (https://onlinelibrary.wiley. |
| [4] | Y. Murata, K. Matsunagi, J. Kashida, Y. Shoji, C. Özen, S. Maeda, T. Fukushima, Angew. Chem. Int. Ed. 2021, 60, 14630-14635. (https://onlinelibrary.wiley. |
| [5] | Y. Shoji, Y. Ikabata, I. Ryzhii, R. Ayub, O. El Bakouri, T. Sato, Q. Wang, T. Miura, B. S. B. Karunathilaka, Y. Tsuchiya, C. Adachi, H. Ottosson, H. Nakai, T. Ikoma, T. Fukushima, Angew. Chem. Int. Ed. 2021, 60, 21817-21823. (https://onlinelibrary.wiley. |
| [6] | J. Kashida, Y. Shoji, Y. Ikabata, H. Taka, H. Sakai, T. Hasobe, H. Nakai, T. Fukushima, Angew. Chem. Int. Ed. 2021, 60, 23812-23818. (https://onlinelibrary.wiley. |