最新の研究
- 2023.11.01
- 吉沢・澤田研究室
ジペプチドを精密に識別する芳香環ナノ道具の開発
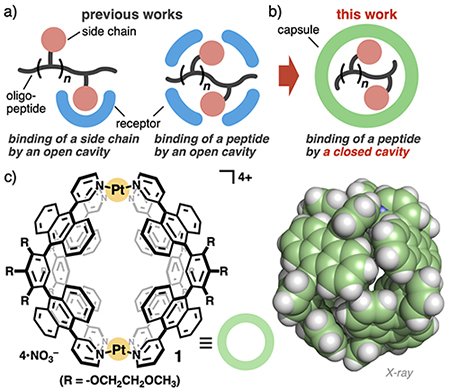
ペプチドはアミノ酸の重合体で、アミノ基とカルボキシ基を両端に持つ生体分子である。天然のアミノ酸だけでも、その個数や種類、結合順序の違いにより、無限に近い数のペプチドが存在する。また、柔軟な鎖状骨格からなり、高い親水性を持つ構造体である。このようなペプチドを「分子レベルで識別する」試みが様々な合成レセプターを使って数多く行われている。その方法は2つに分類できる。1つは標的ペプチドの1~2残基を捕捉することで識別するタイプ(図1a, 左)ともう1つはペプチドのほぼ全体を取り込むことで識別するタイプである(図1a, 右)。しかしながら、これまでの合成レセプターでは「開放的」な内部空間を利用しているため、複雑なペプチド構造のわずかな鎖長と側鎖の違いを厳密に区別できない[1]。
 |
|
| 図1 |
ペプチドの識別方法:a)これまでの合成レセプターの「開放空間」によるペプチドの識別とb)芳香環カプセルの「密閉空間」によるペプチドの識別.c)芳香環カプセル1とその結晶構造(親水基Rは省略)
|
これまでに私達の研究室では、独自に設計した水溶性の芳香環カプセル1(図1c, 左)が、合成分子だけでなく種々な生体分子を捕捉できることを見出している。このカプセルは、湾曲型の有機分子と金属イオンを混合するのみで組み上がる[2]。その内部には、複数の芳香環パネルに囲まれた直径1.3 nm、体積580 Å3の球状空間が存在する。その球状骨格には約0.3 nmの小さな隙間が4つあり、ここから分子を出し入れできる(図1c, 右)。既に、この擬似的な「密閉空間」内で、効率的な分子間相互作用により、疎水性の生体分子(ステロイドホルモンや不飽和脂肪酸、テルペンなど)[3]や親水性の生体分子(糖や乳酸オリゴマーなど)[4]の識別に成功している。
今回、芳香環カプセル1の「密閉空間」に着目し、その内部での多点相互作用を活用することで、特定のペプチドの捕捉に挑戦した(図1b)。その結果、約1 nmの密閉空間に最適な鎖長と側鎖を持つジペプチドの選択的な識別に成功した。また、理論計算と等温滴定カロリメトリー(ITC)測定により、識別メカニズムを明らかにした。さらに、混合物中から標的ジペプチドの蛍光検出を達成した。以下にその詳細を紹介する[5]。
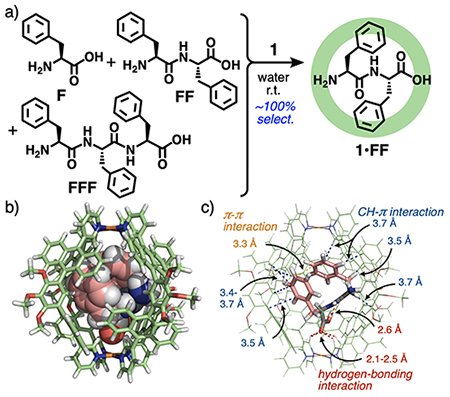
まず、芳香環カプセル1は、水中・室温でフェニルアラニン(F)とその2量体(FF)と3量体(FFF)の混合物中から、ジペプチドFFを100%の選択性で捕捉できることを明らかにした(図2a)。その1H NMRスペクトルでは、内包されたFFの脂肪族シグナルが高磁場に観測された。ESI-TOF MSスペクトルでは、内包体1•FFに由来する分子イオンピークが観測され、「鎖長」の識別によるFFの選択的捕捉を達成した。内包体の理論計算(DFT)から、折り畳まったFFのサイズと形がカプセルの球状空間に適合し、ホスト-ゲスト間で水素結合とCH-π相互作用が効率良く働くことが示された(図2b,c)。
 |
|
| 図2 |
芳香環カプセル1による「鎖長」の識別:a)混合物中からのフェニルアラニンのジペプチドFFの選択的捕捉とb,c)内包体1•FFの計算構造
|
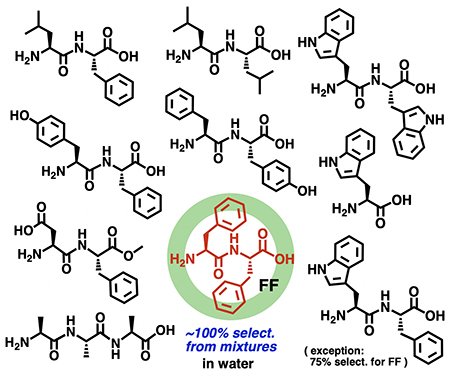
次に、ジペプチド骨格上の「芳香族」と「脂肪族」の側鎖の識別能について解明した。FFとロイシン-フェニルアラニン(LF)とロイシン2量体(LL)を含む3種類のジペプチドの混合物から、FFが100%の選択性で捕捉されることをNMRとMS分析で明らかにした(図3)。さらに、類似した「芳香族」と「芳香族」の側鎖の識別能を明らかにした。実際に、FFとチロシン-フェニルアラニン(YF)の混合物から、1つの水酸基の有無を識別して、カプセル1はFFを100%の選択性で捕捉した。また、FFとトリプトファン-フェニルアラニン(WF)とトリプトファン2量体(WW)の混合物から、カプセル1はFFを75%の選択性で捕捉できた。
 |
|
| 図3 |
芳香環カプセル1による「側鎖」の識別:種々の脂肪族と芳香族側鎖を持つジペプチドからのFFの選択的捕捉
|
高選択性のメカニズムを解明するため、ITC測定により熱力学的パラメータを求めた。その結果、1•FFの形成による結合定数 Ka = 1.07 × 105 M-1、エンタルピー変化ΔH = -11.7 kJ mol-1、エントロピー変化TΔS = 17.0 kJ mol-1、ギブスの自由エネルギー変化ΔG = -28.7 kJ mol-1が見積もられた。これらのデータから、内包挙動はエントロピーおよびエンタルピー駆動であることが示された。一方、1とFの相互作用はITC測定で観測されなかった。
最後に、標的ペプチドの蛍光検出に成功した。フェニルアラニンの1〜3量体の混合物の水溶液に、芳香環カプセル1と蛍光色素のクマリン153を添加した場合、溶液は弱い発光性を示した。一方で、ジペプチドFFを含まない混合溶液では、強い発光性が観測された。すなわち、特定のジペプチドの選択的な検出を達成した。
以上のように、本研究では水中での芳香環カプセルによるジペプチドの精密な識別および高感度な検出を達成した。今後は、種々のペプチドや他の生体分子の識別を目指して、標的に合わせたオーダーメイドな「芳香環ナノ道具」を開発して行きたい。
| [1] | L. Catti, R. Sumida, M. Yoshizawa, Coord. Chem. Rev. 2022, 460, 214460. |
| [2] | N. Kishi, Z. Li, K. Yoza, M. Akita, M. Yoshizawa, J. Am. Chem. Soc. 2011, 133, 11438-11441. |
| [3] | 1) M. Yamashina, T. Tsutsui, Y. Sei, M. Akita, M. Yoshizawa, Science Adv. 2019, 5, eaav3179; 2) K. Niki, T. Tsutsui, M. Yamashina, M. Akita, M. Yoshizawa, Angew. Chem. Int. Ed. 2020, 59, 10489-10492; 3) H. Dobashi, L. Catti, Y. Tanaka, M. Akita, M. Yoshizawa, Angew. Chem. Int. Ed. 2020, 59, 11881-11885; 4) R. Sumida, Y. Tanaka, K. Niki, Y. Sei, S. Toyota, M. Yoshizawa, Chem. Sci. 2021, 12, 9946-9951. |
| [4] | 1) M. Yamashina, M. Akita, T. Hasegawa, S. Hayashi, M. Yoshizawa, Science Adv. 2017, 3, e1701126; 2) S. Kusaba, M. Yamashina, M. Akita, T. Kikuchi, M. Yoshizawa, Angew. Chem. Int. Ed. 2018, 57, 3706-3710. |
| [5] | M. Shuto, R. Sumida, M. Yuasa, T. Sawada, M. Yoshizawa, A Closed Cavity Strategy for Selective Dipeptide Binding by a Polyaromatic Receptor in Water, JACS Au 2023, 3, 2905-2911.(リンク:https://pubs.acs.org/doi/10.1021/jacsau.3c00484) |



