最新の研究
- 2017.02.01
- 西山・三浦研究室
高分子-siRNA結合体におけるリンカーのデザインと生物活性制御
siRNA(small interfering RNA)は20-22塩基対の2本鎖の核酸であり、細胞内においては自身と相補的な配列のmRNA(messenger RNA)を切断することで、タンパク質への翻訳を抑制します(遺伝子発現抑制)[1]。遺伝子発現抑制における配列特異性により、病気の原因となる遺伝子のみを選択的に狙い打つことが出来るため、siRNAは副作用の少ない治療薬としての展開が期待されています。
一方で、siRNAは化学修飾を施すことでさらに性能を向上させることが出来ます。例えば、病変部位の細胞に取り込まれやすくしたり[2]、血液中で(病変部位に届く前に)酵素に分解されにくくすることも出来ます[3]。なかでも、複数の機能を有する高分子でsiRNAを修飾すると、一度に複数の機能をsiRNAに付与することが出来るため、より強力な治療薬へと展開出来ます[4]。しかし、高分子はサイズが大きいため、siRNAが細胞内で遺伝子発現抑制を誘導する際に邪魔になることがあります[5]。siRNAは細胞内の他のタンパク質と相互作用することで新しい複合体を形成し(RNA-induced silencing complex、RISC)、形成されたRISCによりmRNAを切断します。高分子がsiRNAに結合したままだと、その排除体積効果によりRISC形成が阻害され、遺伝子発現抑制を誘導出来なくなります。そこで、一般には、細胞内選択的に切断し高分子とsiRNAとが遊離するような化学リンカーが求められます。
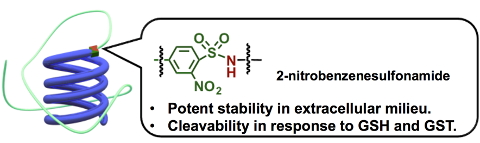 (図1 2-nitrobenzenesulfonamide結合を有する高分子-siRNA結合体)
(図1 2-nitrobenzenesulfonamide結合を有する高分子-siRNA結合体)
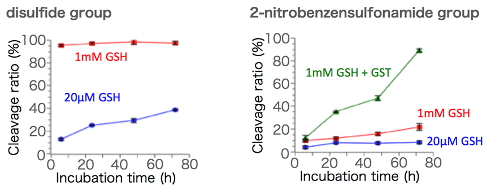 (図2 還元環境下での化学リンカー切断率)
(図2 還元環境下での化学リンカー切断率)
細胞内選択的に切断する化学リンカーとして、最もよく用いられるのはジスルフィド結合です。細胞内は細胞外に比べてより還元的な環境を有しており、その例として、細胞外に比べて細胞内は還元性チオール基を有するグルタチオン(GSH)の濃度が~1000倍高いことが挙げられます。これに関し、ジスルフィド結合は細胞内の高い還元性に応答して切断するのですが、同時に細胞外の穏やかな還元環境でも切断されるという課題がありました。そこで我々は、新しい化学リンカーとして2-nitrobenzenesulfonamide結合に着目しました(図1)。この結合は、1級アミン、2級アミンの保護基としての有用性が知られており、チオール基の求核反応により切断されます。さらに、細胞内特異的に存在するグルタチオン-S-トランスフェラーゼ(GST)は、GSH内のチオール基の求核性を高めることが知られており、2-nitrobenzenesulfonamide結合の細胞内選択的な切断の促進へと繋がります。実際に、2-nitrobenzenesulfonamide結合を用いて高分子-siRNAを調製し、細胞内外における還元環境での切断性を確認したところ、細胞外環境(20 μM GSH)においてはジスルフィド結合の系に比べて安定性が飛躍的に向上しました(図2)。さらに、細胞内還元環境に相当するGSH濃度(1 mM)では緩やかに切断されていたのに対し、GSTと共存されることで切断が促進されました。このことから、2-nitrobenzenesulfonamide結合は、細胞内選択的に存在するGSHとGSTとの共同作用に応答して切断されるリンカーとしての機能が実証されました。また、培養細胞において、2-nitrobenzenesulfonamide結合を有する高分子-siRNA結合体は細胞内にて切断されない化学リンカーを有する高分子-siRNA結合体に比べて高い遺伝子発現抑制能を示したことからも、2-nitrobenzenesulfonamide結合の細胞内での切断は確認されています。これは、細胞内選択的に切断される化学リンカーとして第一選択肢とされてきたジスルフィド結合を超える細胞内選択性を有する新しい化学リンカーの発見であり、高分子-siRNAに関わらず種々の医薬や生体材料への応用が期待出来ます[6]。
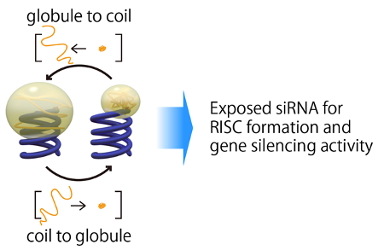 (図3 高分子のcoil-globule転移と遺伝子発現抑制のイメージ)
(図3 高分子のcoil-globule転移と遺伝子発現抑制のイメージ)
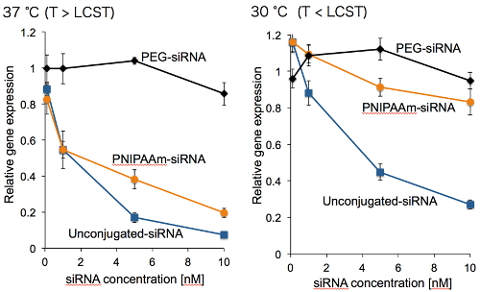 (図4 培養細胞での遺伝子発現抑制試験の結果)
(図4 培養細胞での遺伝子発現抑制試験の結果)
一方で、高分子の排除体積効果によるsiRNAのRISC形成阻害は、上手に使うとsiRNAの遺伝子発現抑制能のコントロールへ展開出来ます。我々は、温度に応じたcoil-globule転移によりサイズが変化するPNIPAAmを用いることで、siRNAの細胞内でのRISC形成能及び遺伝子発現抑制能を制御する手法を考案しました(図3)。PNIPAAmは、LCST(lower critical solution temperature)以下ではcoil状となり、大きい排除体積効果を有しますが、LCST以上ではglobule状となり、排除体積効果が小さくなります。この体積変化に伴い、RISC形成において重要なAgo2(Argonaute2)とsiRNAとの相互作用をON/OFFすることが出来、遺伝子発現抑制能の制御へと繋がります。実際に、LCST以下の温度(30℃)ではPNIPAAm-siRNAとAgo2との相互作用は抑制されていた(遺伝子発現抑制能が低下)のに対し、LCST以上の温度(37℃)ではAgo2との相互作用及び遺伝子発現抑制が通常のsiRNAと同様に誘起されました(図4)。今回用いた温度範囲ではcoil-globule転移を示さないPEGとsiRNAとの結合体(PEG-siRNA)は両方の温度においてAgo2との相互作用及び遺伝子発現抑制能が抑制されていたことから、PNIPAAmのcoil-globule転移に基づいた遺伝子発現抑制能のON/OFF制御が実証されました。このように、siRNA周囲の微小な環境を高分子の構造変化に基づいて制御することで、siRNAの薬理活性をコントロール出来ます。この手法に基づき、特定の細胞内の環境に応じてcoil-globule転移を起こす高分子を分子設計することで、病変細胞への高い選択性をもって薬効を示す高機能性siRNA誘導体へと展開が出来ます[7]。
このように、高分子-siRNA結合体において、高分子由来の排除体積効果を回避するのも重要ですが、それを逆に利用することでsiRNAの活性をコントロール出来ることもわかりました。今回紹介した系において、現在は実際の生体内での挙動の評価を行っています。
参考文献
[1] Elbashir, S. M.; Harborth, J.; Lendeckel, W.; Yalcin, a; Weber, K.; Tuschl, T. Nature 2001, 411, 494.
[2] Nair, J. K.; Willoughby, J. L.; Chan, A.; Charisse, K.; Alam, M. R.; Wang, Q.; Hoekstra, M.; Kandasamy, P.; Kel'in, A. V.; Milstein, S.; Taneja, N.; O'Shea, J.; Shaikh, S.; Zhang, L.; van der Sluis, R. J.; Jung, M. E.; Akinc, A.; Hutabarat, R.; Kuchimanchi, S.; Fitzgerald, K.; Zimmermann, T.; van Berkel, T. J.; Maier, M. A.; Rajeev, K. G.; Manoharan, M. J. Am. Chem. Soc. 2014, 136, 16958.
[3] Lee, S. H.; Mok, H.; Park, T. G. Macromol. Biosci. 2011, 11, 410.
[4] Rozema, D. B.; Lewis, D. L.; Wakefield, D. H.; Wong, S. C.; Klein, J. J.; Roesch, P. L.; Bertin, S. L.; Reppen, T. W.; Chu, Q.; Blokhin, A. V.; Hagstrom, J. E.; Wolff, J. A. Proc. Natl. Acad. Sci. U. S. A. 2007, 104, 12982.
[5] Takemoto, H.; Miyata, K.; Hattori, S.; Ishii, T.; Suma, T.; Uchida, S.; Nishiyama, N.; Kataoka, K. Angew. Chem., Int. Ed. 2013, 52, 6218.
[6] Huang, C. H.; Takemoto, H.; Nomoto, T.; Tomoda, K.; Matsui, M.; Nishiyama, N. ChemMedChem 2017, 12, 19.
[7] Harun, N. F. C.; Takemoto, H.; Nomoto, T.; Tomoda, K.; Matsui, M.; Nishiyama, N. Bioconjugate Chem. 2016, 27, 1961.



